

La gran explosión tecnológica, el sedentarismo laboral y la mayor accesibilidad a productos hipercalóricos son algunos de los responsables de la alta prevalencia de la obesidad en las sociedades actuales. La incidencia de la obesidad se ha duplicado desde el año 1980, llegando a alcanzar más de 600 millones de adultos obesos en el año 2014 en todo el mundo [1]. En poco tiempo, el contexto de escasez alimenticia y elevadas demandas calóricas ha ido cediendo paso a un ambiente con un abundante suministro calórico pero escasas demandas energéticas, lo que ha derivado en este desbalance. Pero lo que resulta realmente preocupante no es la obesidad como un problema meramente estético, sino el riesgo que ésta supone para el desarrollo de múltiples enfermedades crónicas, tales como las enfermedades cardiovasculares, la diabetes mellitus de tipo 2, el hígado graso, desórdenes músculo-esqueléticos y el cáncer [2]. De hecho, muchas de estas enfermedades se encuentran entre las principales causas de muerte a nivel mundial, de ahí que la obesidad sea considerada la segunda causa prevenible de muerte tras el tabaquismo [3].
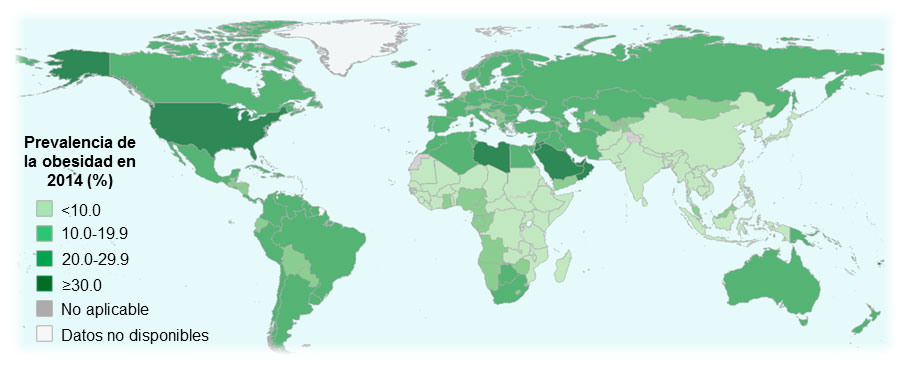
Fuente: modificado de Organización Mundial de la Salud (OMS) (2015).
Debido a que la obesidad se desarrolla cuando la ingesta calórica sobrepasa al gasto energético, la lucha contra esta epidemia se ha centrado en tratar de comprender los mecanismos que regulan estos dos elementos, con la finalidad de desarrollar nuevas terapias que persigan su control. Hasta el momento, se han propuesto diversos tratamientos farmacológicos para lograr la pérdida de peso por medio de una reducción en la ingesta alimenticia, así como se está tratando de comprender los mecanismos moleculares que regulan el gasto energético. Puesto que el gasto energético es la suma del metabolismo basal (la cantidad de energía que se gasta en una situación de reposo), la termogénesis (la generación de calor debido al procesamiento de los alimentos ingeridos) y la actividad física [4], actuando sobre cualquiera de estos tres elementos se puede conseguir una disminución de la acumulación de grasa corporal.
Con la finalidad de diseñar nuevas terapias para el tratamiento de la obesidad y sus patologías asociadas, es preciso conocer las diversas vías de señalización que contribuyen a la misma. Una de estas vías es la de las proteínas quinasas activadas por estrés (SAPKs). Estas proteínas son esenciales para responder al estrés metabólico y, por tanto, pueden contribuir a la patogénesis de la obesidad [5]. La obesidad se caracteriza por un estado inflamatorio acompañado de altos niveles de citoquinas proinflamatorias (proteínas que desempeñan importantes papeles promoviendo la inflamación) y de ácidos grasos libres circulantes, que causan la activación de mecanismos inducidos por estrés en la célula, tales como las mencionadas SAPKs [6].
Se han identificado dos grupos de SAPKs en mamíferos: JNK (c-Jun N-terminal kinases) y p38 MAPKs (p38 mitogen-activated protein kinases) [7]. Mientras que el papel de JNK en la obesidad y en la resistencia a la insulina (y consecuente diabetes) se ha estudiado en profundidad [8], las implicaciones de p38 en este contexto son menos conocidas.
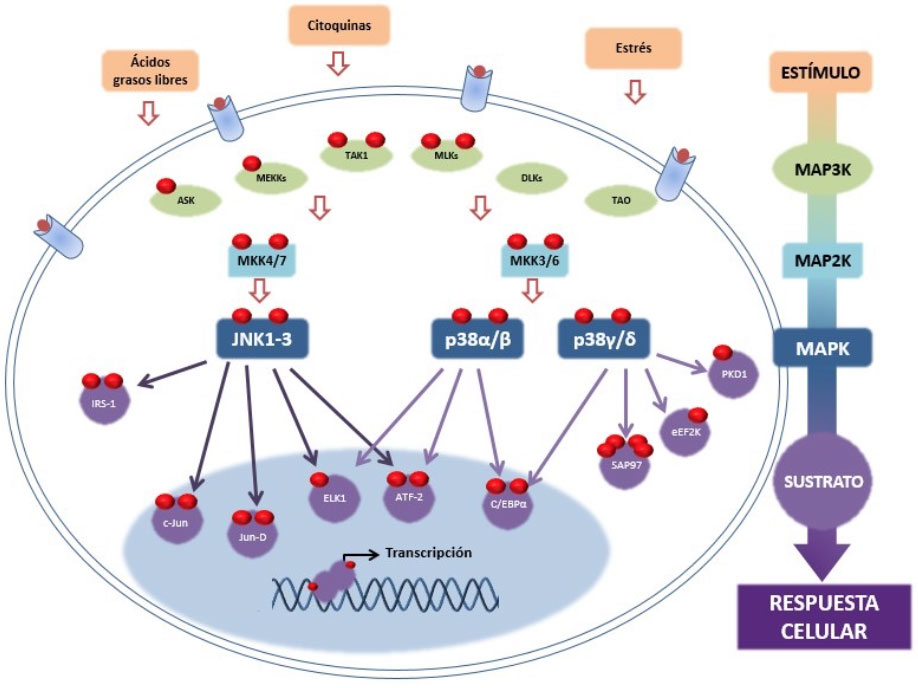
Vía de señalización de las proteínas quinasas activadas por estrés. Como todos los miembros de la familia de las MAPKs (proteínas quinasas activadas por mitógenos), las SAPKs, JNKs y p38s, se activan por una cascada de fosforilación. Algunos estímulos que son abundantes en contextos de obesidad, tales como citoquinas y ácidos grasos libres, son capaces de activar a estas proteínas. La activación de las mismas finaliza con la fosforilación de sustratos específicos, induciendo la respuesta celular en función del estímulo inicial. Fuente: modificado de Manieri & Sabio, Journal of Molecular Endocrinology (2015).
Se conocen cuatro miembros de la familia de p38 MAPKs, con distintos patrones de expresión tisular: p38α, que se expresa en la mayoría de los tipos celulares; p38β, fundamentalmente en el cerebro; p38γ, ubicua y con altos niveles de expresión en el músculo esquelético; y p38δ, que se expresa principalmente en neutrófilos y glándulas endocrinas [9]. p38α es la isoforma más estudiada, puesto que desempeña importantes funciones en la homeostasis tisular (adecuado mantenimiento de los tejidos del organismo), así como en diversas patologías tales como la inflamación y la respuesta inmune, el cáncer, enfermedades cardiacas y neurodegenerativas [10]. La deficiencia de p38α es letal, produciendo defectos en la organogénesis de la placenta [11]. Por este motivo, para estudiar el papel de esta quinasa en ratones adultos es preciso utilizar modelos condicionales en los que la proteína se pierda exclusivamente en determinados órganos. Asimismo, estos modelos animales son necesarios para conocer el papel exacto que las distintas isoformas de p38 desempeñan en cada órgano. En el caso de la obesidad, resulta de especial interés comprender las funciones que estas quinasas desempeñan en aquellos órganos que tienen una implicación directa en el metabolismo y, por tanto, son esenciales para el mantenimiento de unas condiciones metabólicas adecuadas que ayuden a prevenir la aparición de la obesidad. Por una parte, numerosos estudios han desvelado el papel de las p38 MAPKs como reguladores de la homeostasis de la glucosa en el hígado, aunque todavía no se conoce el papel que desempeña cada isoforma en este órgano [12]. Por el contrario, otros estudios se han centrado en comprender cuál es la función que estas proteínas tienen en el tejido adiposo, inicialmente considerado como un órgano con la única función de almacenamiento de grasa, pero cuyas funciones e implicaciones a nivel sistémico gozan de una mayor relevancia, siendo considerado en la actualidad un órgano endocrino que secreta numerosas adipoquinas que controlan el metabolismo. Dentro del tejido adiposo encontramos el tejido adiposo blanco (TAB), que almacena el exceso de energía como triglicéridos, y el tejido adiposo marrón (TAM), especializado en la disipación de energía a través de la producción de calor. Se ha descrito que las p38 MAPKs regulan la diferenciación de ambos tipos de tejido adiposo [13]: por ejemplo, p38α regula la diferenciación del TAM mediante el control de los niveles de expresión de la proteína UCP1 (uncoupling protein 1) [14,15]. Esto ha abierto nuevas perspectivas para el tratamiento de la obesidad, puesto que logrando una mayor actividad del TAM se podría incrementar el gasto energético y, en consecuencia, lograr una reducción del peso corporal [16]. Durante muchos años se ha pensado que este tejido sólo estaba presente en pequeños mamíferos y en recién nacidos, ayudando a la supervivencia frente a bajas temperaturas. Sin embargo, recientemente se ha observado la presencia de TAM metabólicamente activo en humanos, especialmente cuando el cuerpo se expone a bajas temperaturas. De este modo, la menor actividad de este tejido en individuos obesos puede contribuir al menor gasto energético que, en este caso, conlleva la aparición de obesidad [17].

Aunque son muchos los estudios que han tratado de determinar el papel de las quinasas del estrés en distintos órganos, todavía quedan muchos interrogantes por resolver. Con cada descubrimiento se incrementa el conocimiento acerca de estas proteínas, pero al mismo tiempo se abren nuevas incógnitas y diferentes perspectivas de estudio que están tratando y tratarán de lograr un único fin: combatir la obesidad.
REFERENCIAS
[1] Organización Mundial de la Salud (OMS) (2015). “Obesidad y sobrepeso”. [En línea]. Disponible en: http://www.who.int/mediacentre/factsheets/fs311/en/.
[2] Speakman, J. R. (2004). Obesity: the integrated roles of environment and genetics. The Journal of Nutrition, 134(8): 2090S-105S.
[3] Kushner, R. F. (2002). Medical management of obesity. Seminars in Gastrointestinal Disease, 13(3): 123-32.
[4] Westerterp, K. R. (2017). Control of energy expenditure in humans. European Journal of Clinical Nutrition, 71(3): 340-4.
[5] Manieri, E., Sabio, G. (2015). Stress kinases in the modulation of metabolism and energy balance. Journal of Molecular Endocrinology, 55(2): R11-22.
[6] Hotamisligil, G. S. (2006). Inflammation and metabolic disorders. Nature, 444(7121): 860-7.
[7] Kyriakis, J. M., Avruch, J. (2012). Mammalian MAPK signal transduction pathways activated by stress and inflammation: a 10-year update. Physiological Reviews, 92(2): 689-737.
[8] Sabio, G., Davis, R. J. (2010). cJun NH2-terminal kinase 1 (JNK1): roles in metabolic regulation of insulin resistance. Trends in Biochemical Sciences, 35(9): 490-6.
[9] Sabio, G., Davis, R. J. (2014). TNF and MAP kinase signalling pathways. Seminars in Immunology, 26(3): 237-45.
[10] Cuadrado, A., Nebreda, A. R. (2010). Mechanisms and functions of p38 MAPK signalling. Biochemical Journal, 429(3): 403-17.
[11] Adams, R. H., et al. (2000). Essential role of p38α MAP kinase in placental but not embryonic cardiovascular development. Molecular Cell, 6(1): 109-16.
[12] Cao, W., et al. (2005). p38 Mitogen-activated protein kinase plays a stimulatory role in hepatic gluconeogenesis. Journal of Biological Chemistry, 280(52): 42731-7.
[13] Engelman, J. A., et al. (1998). Specific inhibitors of p38 mitogen-activated protein kinase block 3T3-L1 adipogenesis. Journal of Biological Chemistry, 273(48): 32111-20.
[14] Cao, W., et al. (2004). p38 mitogen-activated protein kinase is the central regulator of cyclic AMP-dependent transcription of the brown fat uncoupling protein 1 gene. Molecular and Cellular Biology, 24(7): 3057-67.
[15] Tseng, Y. H., et al. (2008). New role of bone morphogenetic protein 7 in brown adipogenesis and energy expenditure. Nature, 454(7207): 1000-4.
[16] Giralt, M., Villarroya, F. (2013). White, brown, beige/brite: different adipose cells for different functions? Endocrinology, 154(9): 2992-3000.
[17] Saely, C. H., et al. (2010). Brown versus white adipose tissue: a mini-review. Gerontology, 58(1): 15-23.

AUTOR
Leticia Herrera
Premio accésit del jurado por el trabajo «Papel de la señalización muscular de p38 MAPK sobre el metabolismo» realizado en la Universidad Autónoma de Madrid bajo la tutela de Guadalupe Sabio Buzo (CNIC).
+INFO CERTAMEN ARQUÍMEDES





No comments yet.