
El cáncer es la segunda causa de muerte y se trata de un conjunto de enfermedades en las que se observa un crecimiento descontrolado de las células del organismo. Suele comenzar de manera localizada, aunque puede diseminarse a otros órganos, en un proceso conocido como metástasis. Específicamente el cáncer de tiroides se inicia en la glándula tiroidea, localizada a ambos lados de la tráquea en la parte inferior del cuello. La incidencia del cáncer de tiroides ha aumentado considerablemente en las últimas décadas, llegándose a triplicar los casos diagnosticados en Estados Unidos comparando con tan solo hace 40 años.
El cáncer de tiroides tiene, por lo general, buena respuesta al tratamiento. Cuando se diagnostica este tipo de cáncer, se extirpa mediante cirugía la glándula tiroidea a los pacientes, que serán posteriormente tratados con hormonas tiroideas durante el resto de su vida, necesarias para el correcto funcionamiento del organismo. Además, para eliminar las células de tiroides restantes o si el cáncer se ha diseminado, se les administra yodo radiactivo por vía oral, que entra y destruye específicamente las células procedentes del tiroides. Sin embargo, aunque en un número reducido de pacientes, existen algunos cánceres que no responden a este tratamiento, siendo las formas más agresivas y peligrosas del cáncer de tiroides. Una vez diagnosticado este tipo específico de cáncer de tiroides, la esperanza media de vida es de unos 6 meses. Por esta razón, la búsqueda de nuevos mecanismos que expliquen la formación y mantenimiento de este cáncer resulta fundamental para obtener nuevas dianas moleculares y nuevos tratamientos.
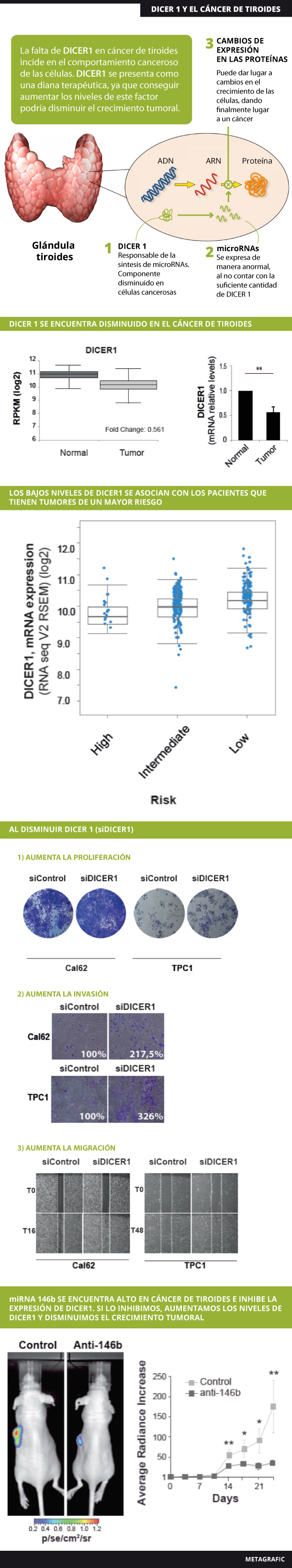
Para que las células realicen sus funciones son necesarias las proteínas. La información para dar lugar a cada proteína se encuentra en el ADN, el cual da lugar a unas moléculas llamadas ARN mensajeros que finalmente darán lugar a las proteínas correspondientes. Recientemente se ha descrito el papel que tienen unas novedosas moléculas reguladoras conocidas como microRNAs. Los microRNAs son pequeños fragmentos de ARN de unos 21 nucleótidos que se unen a los ARN mensajeros e impiden la producción de la proteína correspondiente, modulando de esta manera las diferentes funciones en las que esas proteínas están implicadas. Un solo microRNA puede unirse a varios ARN mensajeros modificando así diversas funciones. Se ha descrito que los microRNAs no solo juegan un papel fundamental para la función normal de la célula, sino que pueden ser importantes para el inicio y desarrollo del cáncer. Si un determinado microRNA se expresa de manera anormal (en exceso o en defecto), se producirán también cambios de expresión de las proteínas a las que afectan, pudiendo dar lugar a cambios en el crecimiento de las células, dando finalmente lugar a un cáncer.
Uno de los componentes fundamentales de la ruta de síntesis de estos microRNAs es DICER1. Esta proteína permite que los microRNAs sean maduros y puedan realizar su función. Se ha visto que DICER1 está disminuido en los pacientes con cáncer de tiroides, específicamente en los grupos de mayor riesgo. En nuestro grupo, dirigido por la doctora Pilar Santisteban, en el Instituto de Investigaciones Biomédicas “Alberto Sols”, hemos confirmado estas observaciones en pacientes y hemos realizado ensayos en células de cáncer de tiroides, demostrando que al eliminar DICER1 se induce un comportamiento más agresivo en estas células, es decir, un aumento de las características propias de las células cancerosas como son proliferación, migración e invasión. Así mismo, si en células con bajos niveles de DICER1 inducimos su expresión disminuirán estas características malignas. Teniendo en cuenta estos datos, una terapia basada en la recuperación o aumento de nuestra diana terapéutica, DICER1, en los pacientes podría interferir en el crecimiento tumoral.
Además, hemos estudiado los mecanismos de regulación de DICER1 más importantes con el fin de entender por qué este factor se encuentra disminuido en cáncer de tiroides. Así hemos demostrado que una importante proteína tiroidea conocida como TTF1 (de las siglas en inglés factor de transcripción de tiroides 1), que se conoce que disminuye en este cáncer, induce la expresión de DICER1. Así al disminuir este factor, también disminuye DICER1. Además, el microRNA más abundante e importante en cáncer de tiroides (el microRNA 146b) inhibe DICER1, explicando también los bajos niveles encontrados. Por tanto, nuestros estudios sugieren que la disminución de DICER1 en cáncer es un evento importante para la progresión de las células tumorales y por ello se encuentra finamente regulado en este tipo de tumores. El estudiar su mecanismo de regulación nos está permitiendo obtener nuevas terapias que permiten el aumento de DICER1, como es la inhibición del microRNA 146b, que está resultando muy beneficiosa en nuestros estudios pre-clínicos en ratones.
Como conclusión, nuestros estudios muestran que la falta de DICER1 en cáncer de tiroides tiene unas consecuencias en el comportamiento canceroso de las células. Por esta razón esta proteína se encuentra muy regulada. Debido a que la disminución de DICER1 se asocia con los pacientes de mayor riesgo, el analizar los niveles de DICER1 en pacientes podría resultar útil para clasificarlos y por tanto para decidir la terapia más adecuada. Por último, DICER1 se presenta como una diana terapéutica, ya que conseguir aumentar los niveles de este factor podría disminuir eficazmente el crecimiento tumoral.

AUTORA
Julia Ramírez-Moya.
Julia Ramírez-Moya ha sido la ganadora del Premio especial al mejor trabajo de investigación sobre el cáncer de la Fundación “Vencer el cáncer” en la XV convocatoria del Certamen Arquímedes y la ganadora del segundo premio de la categoría ciencias biológicas y biomédicas en el mismo certamen. Julia Ramírez, alumna de la Universidad Autónoma de Madrid, recibió esta distinción por su trabajo “Papel de la maquinaria de biogénesis de microRNAs en cáncer de tiroides” tutorizado por Pilar Santisteban Sanz (Consejo Superior de Investigaciones Científicas).
+INFO CERTAMEN ARQUÍMEDES
Web del certamen | Facebook





No comments yet.