
El fet de menjar el que et vinga en gana i no engreixar, a qui no li agradaria? Encara que només siga perquè ens arruïna l’operació biquini, ja sabem que abusar dels greixos en la nostra dieta no ens fa cap bé. Però arribar a tindre sobrepés o obesitat té moltes altres conseqüències negatives al nostre organisme, encara que no siguen tan fàcils de detectar a simple vista com un mixelín.
Per exemple, ser obés fa que augmente la probabilitat que patim diabetis, hipertensió, síndrome del fetge gras o fins i tot alguns tipus de càncer, entre altres malalties. Tot i això, el nombre de persones amb sobrepés o obesitat ha augmentat de manera dramàtica durant les últimes dècades, a causa, principalment, de la nostra forma de vida sedentària i de la nostra alimentació. Per tot això, al nostre laboratori estem interessats a previndre les conseqüències nocives associades a l’obesitat –i potser hàgem trobat una manera de combatre’n algunes: disminuir els nivells de GRK2.
Què és GRK2? És una proteïna que tenim a totes les cèl·lules del nostre organisme, coneguda per fosforilar (modificar) certs receptors cel·lulars per a dessensibilitzar-los. A més, estudis previs van relacionar aquesta proteïna amb la insulina: GRK2 atenuaria els efectes que té la insulina a les nostres cèl·lules, ja que hi interacciona i així segresta una altra proteïna necessària perquè la insulina funcione correctament.
Per què això és important en l’obesitat? La insulina és una hormona que s’encarrega de regular el metabolisme. La pèrdua de sensibilitat a la insulina o insulinoresistència és la condició que es dóna quan el cos no respon a aquesta hormona, per la qual cosa aquesta no exerceix els seus efectes i el metabolisme deixa de regular-se adequadament. La insulinoresistència és una de les conseqüències de l’obesitat i, per la relació que acabem de comentar, GRK2 podria estar contribuint al fet que s’adquirira.
Això ens va portar a plantejar la hipòtesi que disminuir els nivells de GRK2 podria ser beneficiós per a atenuar la insulinoresistència provocada per la dieta, i així atenuar les conseqüències nocives d’aquesta.
Com comprovem això? Per sort per a nosaltres i per desgràcia per a ells, els ratolins no es lliuren de l’obesitat: comprovem que quan s’alimenten amb una dieta alta en greix, guanyen més pes i adquireixen insulinoresistència. Això fa que puguem utilitzar-los per a l’estudi de l’obesitat. Centrem aquest estudi en el fetge, perquè és un òrgan clau en la regulació del metabolisme i perquè una altra de les conseqüències d’aquesta dieta és l’acumulació de greix en aquest òrgan, com també comprovem. A més, també vam observar que els nivells proteics de GRK2 augmentaven al fetge a conseqüència de la dieta.
Per a comprovar la nostra hipòtesi i veure si GRK2 estava tenint alguna cosa a veure en l’aparició d’aquestes conseqüències, vam crear un ratolí transgènic que posseïa la meitat de GRK2 a totes les cèl·lules del cos que un ratolí normal. I, efectivament, vam veure que aquests ratolins transgènics no guanyaven tant de pes amb la dieta ni perdien la sensibilitat a la insulina ni acumulaven greix al fetge. A més, mantenien els nivells de GRK2 estables tot i la dieta alta en greix.
En canvi, aquests efectes protectors es perdien quan la dieta es prolongava fins a 33 setmanes en lloc de 12: a llarg termini, sí que augmentava la quantitat de GRK2 en aquests ratolins, i començaven a guanyar pes, es tornaven insulinoresistents i presentaven acumulació de greix al fetge.
Per a estudiar a què era deguda l’acumulació o no de greix al fetge que estàvem observant en les diferents condicions, vam estudiar els nivells d’algunes proteïnes clau en el metabolisme de lípids al fetge, la qual cosa podia indicar-nos el flux de certs processos metabòlics. Vam observar una bona correlació entre els nivells de FAS, proteïna encarregada de sintetitzar lípids de novo, i el grau d’acumulació de lípids al fetge. El mateix ocorria amb CD36, proteïna encarregada d’introduir àcids grassos a l’interior cel·lular. Això ens va indicar que l’acumulació de greix observada podia ser deguda al fet que les cèl·lules hepàtiques sintetitzen més lípids i capten més àcids grassos de la sang. Sorprenentment, també vam observar un augment en una altra proteïna anomenada HADHA, la qual cosa indicaria que les cèl·lules estarien oxidant (consumint) més àcids grassos. Això no quadrava amb els resultats que hem comentat. No obstant això, cal tindre en compte que aquest procés, en condicions com les que produeix la dieta alta en greix, pot estar inhibit per mitjà d’altres mecanismes, per la qual cosa, encara que augmente l’HADHA, pot no estar produint-se un augment en l’oxidació de lípids.
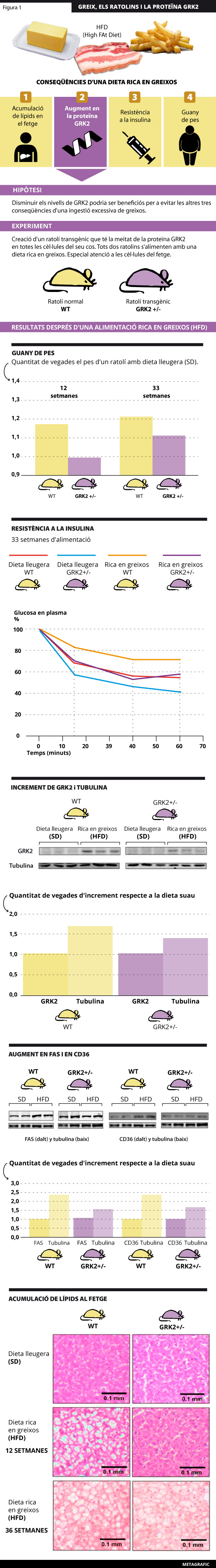
Fig. 1. Es mostren les conseqüències que han sorgit en alimentar els ratolins normals (WT) i transgènics (GRK2+/-) amb una dieta alta en greix. Aquestes conseqüències es poden resumir en: augment de pes, desenvolupament de resistència a la insulina, augment en l’acumulació de lípids al fetge (a causa de l’augment de FAS i CD36) i increment en els nivells de GRK2 al fetge. Una dieta alta en greix fa que els ratolins normals presenten característiques patològiques. En canvi, els ratolins GRK2+/- estan protegits d’aquest efecte només quan aquesta dieta dura 12 setmanes, però no quan en dura 33. Això indica que la dieta alta en greix augmenta els nivells de GRK2, i quan arriben a un cert llindar, GRK2 contribueix o agreuja les conseqüències patològiques de la dieta.
En resum, la dieta alta en greix no fa cap bé a l’organisme i, a més, fa que augmenten els nivells de GRK2, una proteïna que al seu torn contribueix o agreuja les conseqüències negatives d’aquesta dieta. El peix que es mossega la cua. Tindre menys nivells de GRK2 fa que la dieta alta en greix siga menys dolenta, però només quan no es prolonga massa temps. En aquest últim cas, tot i ser un transgènic que expressa la meitat de GRK2 i per això està protegit dels efectes nocius del greix, els nivells d’aquesta proteïna comencen a augmentar, per la qual cosa es perd aquest estat de protecció.
Deduïm d’aquest estudi la importància d’utilitzar models científics adequats quan estem estudiant patologies humanes: el model de 33 setmanes és més semblant al que ocorreria en humans obesos, i veiem que molecularment no és igual estar 12 setmanes que 33 menjant greix. Perquè, per exemple, no observem un augment de GRK2 en els nostres ratolins transgènics a les 12 setmanes, però sí a les 33.
I el més important: d’aquest estudi concloem que disminuir o potser inactivar GRK2 podria utilitzar-se com a estratègia per a previndre les patologies derivades d’una dieta alta en greix. Però fins que aquesta teoria arribe a validar-se i es desenvolupen fàrmacs contra GRK2, millor deixar de fartar-se de creïlles fregides i hamburgueses. El teu fetge t’ho agrairà.

AUTORA
Irene Herranz Montoya
Accèssit del Jurat al treball: “Efecte de GRK2 a l’esteatosi hepàtica en model murins de
obesitat induïda per dieta alta en greix a mig i llarg termini: conseqüències fisiopatològiques “. Universitat Autònoma de Madrid. Tutor: Federico Mayor Menéndez.
+INFO CERTAMEN ARQUÍMEDES
Web del certamen | Facebook






No comments yet.